КЛІНІЧНЕ ДОСЛІДЖЕННЯ HOHOEMI
Багатоцентрове відкрите дослідження еміцизумабу, який застосовувався кожні 2 або 4 тижні у дітей з важкою гемофілією А без інгібіторів¹
У багатоцентровому відкритому дослідженні (HOHOEMI) оцінювали ефективність, безпечність та фармакокінетику еміцизумабу у пацієнтів молодше 12 років (Японія), які страждають на важку гемофілію А без інгібіторів до фактора VIII (FVIII)¹.
Дизайн
Еміцизумаб вводився підшкірно у вигляді чотирьох навантажувальних доз (3 мг/кг) щотижня, з наступним введенням підтримуючих доз (3 мг/кг) кожні два тижні (Q2W) або 6 мг/кг кожні 4 тижні (Q4W) у 6 і 7 пацієнтів відповідно.
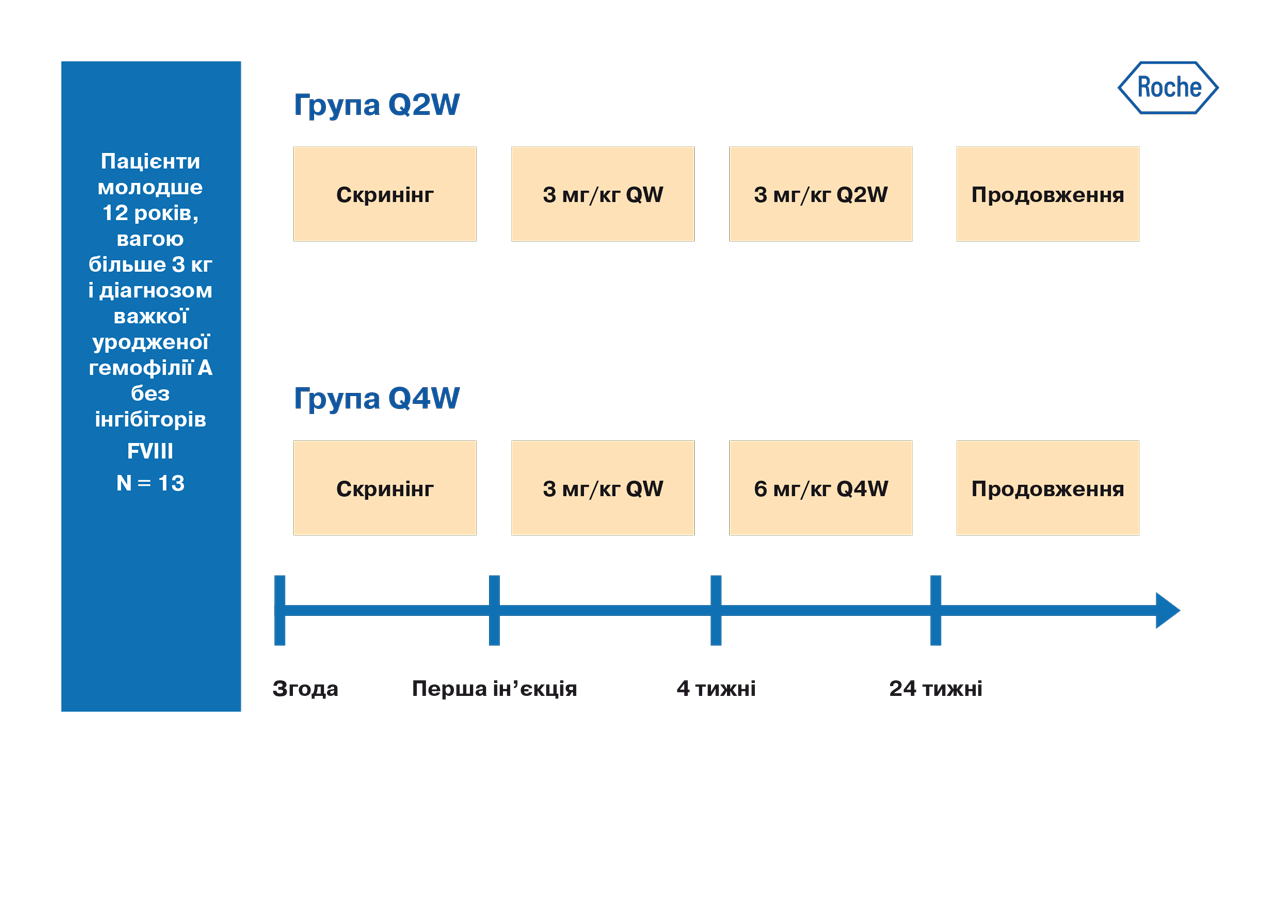
Результати
У когортах Q2W і Q4W у 2/6 та 5/7 пацієнтів не спостерігалося ніяких кровотеч, а співвідношення щорічних показників кровотеч до кількості лікованих кровотеч склало 1,3 (95% довірчий інтервал [CI], 0,6–2,9) і 0,7 (95% CI, 0,2–2,6) відповідно.
Усі батьки (або піклувальники) надали перевагу еміцизумабу над попереднім лікуванням.
Спостерігався лише один побічний ефект (реакція в місці ін’єкції).
Тромбоемболічних ускладнень або тромботичних мікроангіопатій не спостерігалося.
Індивідуальні концентрації еміцизумабу в плазмі були в межах мінливості, яка спостерігалася у попередніх дослідженнях для дорослих і підлітків.
Усі пацієнти показали негативний результат тесту на антитіла проти еміцизумабу.
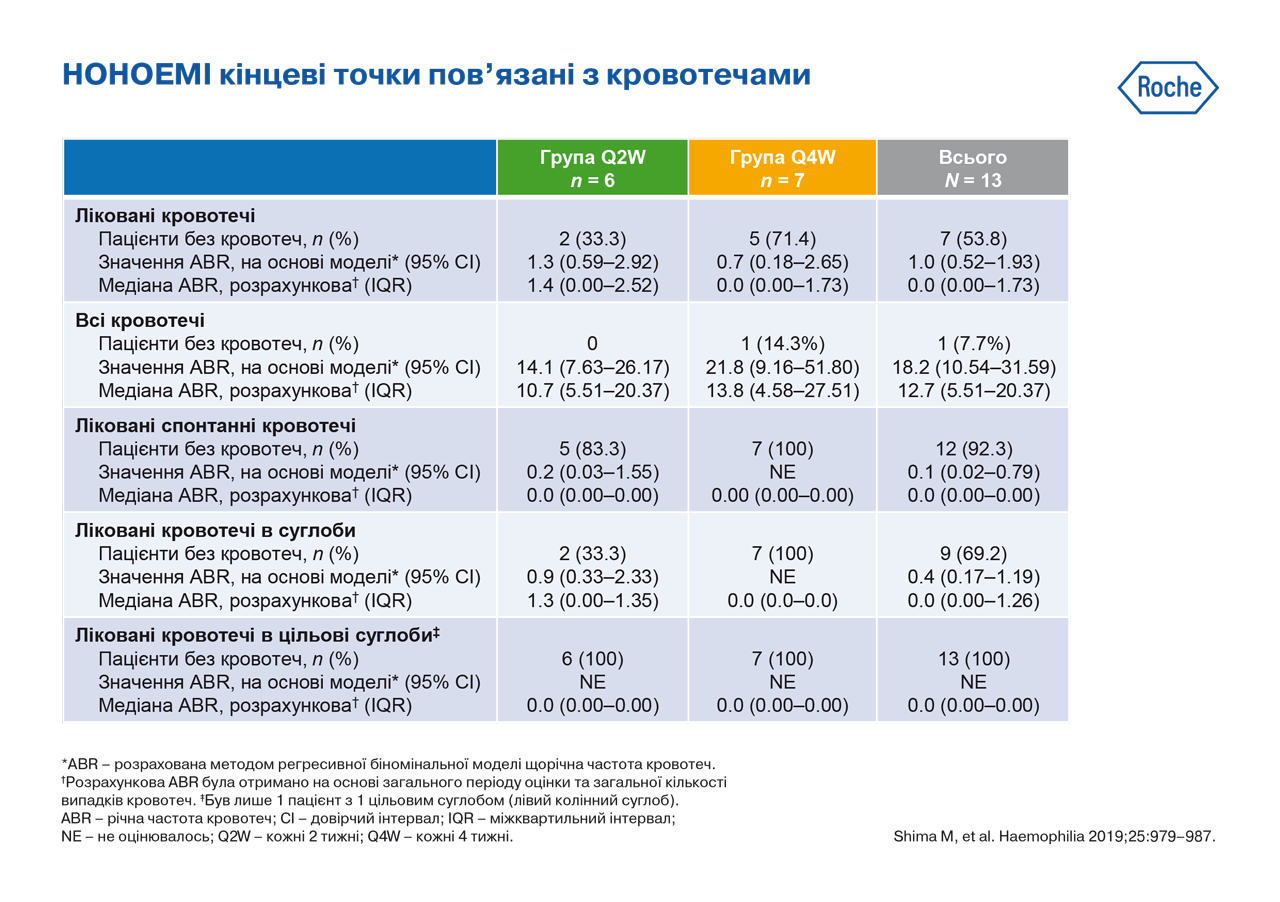
Висновок
Еміцизумаб, який застосовувався у дозах Q2W або Q4W, виявився ефективним і безпечним у дітей, які страждають на важку гемофілію А без інгібіторів.
ЛІТЕРАТУРА
- Shima M, et al. Haemophilia 2019;25:979–987.

